ARTÍCULO ESPECIAL
En el mes de la concesión de los Premios Nobel, rendimos homenaje a Alfred Nobel y a los galardonados con el Premio de Fisiología y Medicina de 2020
In the month of the Nobel Prize Awards, we pay tribute to Alfred Nobel and to the recipients of the 2020 Prize in Physiology and Medicine
Francisco J. Sánchez-Muniz1, Jesús M Culebras2, Luis Vicente-Vacas3
1 Catedrático Emérito de Nutrición. Facultad de Farmacia de la Universidad Complutense de Madrid y Académico de número de la Real Academia Nacional de Farmacia, España
![]() https://orcid.org/0000-0002-2660-5126
https://orcid.org/0000-0002-2660-5126
2De la Real Academia de Medicina de Valladolid y del IBIOMED, Universidad de León. Miembro de Número y de Honor de la Academia Española de Nutrición y Dietética. Académico Asociado al Instituto de España. AcProfesor Titular de Cirugía. Director, Journal of Negative & No Positive Results. Director Emérito de NUTRICION HOSPITALARIA, España
![]() https://orcid.org/0000-0003-3234-6957
https://orcid.org/0000-0003-3234-6957
3 Editor de Journal of Negative & No Positive Results. España
![]() https://orcid.org/0000-0002-4701-4149
https://orcid.org/0000-0002-4701-4149
* Autor para correspondencia.
|
|
Attribution-NonCommercial-ShareAlike 4.0 International License La revista no cobra tasas por el envío de trabajos, |
|
Es este artículo una continuación del homenaje que JONNPR dio a Alfred Nobel y a los galardonados con el Premio Nobel de Fisiología y Medicina en previas ediciones de 2017, 2018 y 2019(1-3). Esta iniciativa no tiene otra finalidad que recordar la importancia que alcanzan en el mundo científico los premios Nobel y poner de manifiesto los méritos que reúnen aquellos a los que el Instituto Karolinska reconoce año a año como merecedores de tan alto galardón. Este año ha recaído sobre los descubrimientos de un aspecto fundamental de la lucha contra un problema de salud mundial, la lucha contra la hepatitis que degenera en cirrosis y cáncer de hígado y que produce 400.000 muertes anuales, siendo además una de las causas más importantes de trasplante hepático(4).
La noticia salió a los medios como siempre el primer lunes del actual mes de octubre, es decir el día 5 pasado por lo que está aún muy reciente la noticia y es merecedora de un homenaje. Como en años anteriores resaltaremos su importancia en el contexto de la ciencia en las últimas décadas, sin olvidar a la figura de Alfred Nobel. Al igual que en la publicación en JONNPR en 2019, queremos recordar en la importancia de rescatar del olvido aquellos Premios Nobel en Fisiología y Medicina que se otorgaron entre los años 2000 y el 2016 y queremos anunciar a nuestros lectores que se encuentra casi presta para su publicación una actualización de la importancia que tuvo y tiene el Premio Nobel concedido en 2009 a las americanas Elizabeth Blackburn, Carol W. Greider y Jack W. Szostak por el descubrimiento de una enzima, la telomerasa, que ayuda a evitar el acortamiento de los cromosomas en cada división celular, jugando un papel esencial evitando el envejecimiento celular(6).
Seis anuncios en seis días han hecho realidad los sueños de muchos científicos y personalidades que optan a estos premios tan prestigiosos y que han comenzado, según establece la tradición, el primer lunes de octubre con el Premio Nobel de Medicina y Fisiología que entrega el Instituto Karolinska de Estocolmo. Han seguido posteriormente el de Física (martes 6), de Química (miércoles 7), de Literatura (jueves 8), de la Paz (viernes 9), cerrando el de Economía (lunes 12). Desafortunadamente, debido a la pandemia del Covid-19, aunque todo parece igual, los anuncios han sido virtuales y con una mínima presencia de periodistas acreditados.
Esta reseña de los medios es antesala de lo que tendrá lugar el diez de diciembre, fecha, que además de ser conmemorativa de la muerte de Alfred Nobel, es en la que tiene lugar la ceremonia de entrega de los premios Nobel y el reconocimiento oficial de los galardonados. Desgraciadamente dicha ceremonia tendrá este año un carácter mucho más restringido, habiéndose suprimido las ceremonias con antiguos galardonados por estos premios, los banquetes, ceremonias y por tanto mucho del boato de otros años.
Como es ya conocido por los medios de comunicación desde que se empezó a conceder el Nobel de Medicina y Fisiología hace 119 años, interrumpida solamente la tradición por las dos grandes guerras mundiales, a primeros de diciembre han ido teniendo lugar la doble ceremonia de los Premios Nobel en el Ayuntamiento de Oslo (donde se entrega el Premio Nobel de la Paz) y, horas más tarde, en el Konserthus de Estocolmo donde se conceden los demás galardones en una sencilla y elegante ceremonia a la que asisten los académicos responsable de la selección final de premiados y la familia real de Suecia(5). No obstante este año se han cancelado las galas correspondientes a Estocolmo para el Premio Nobel de la Paz y en Oslo se reserva un espacio muy reducido para los asistentes en la Universidad. Como curiosidad, el premio Nobel de Medicina lo han ganado 219 personas, de las cuales solo 12 son mujeres.
Este año, a parte de las cancelaciones de los banquetes y conciertos, vendrán otras novedades. Como ya hemos comentado la ceremonia del diez de Diciembre de Estocolmo ya ha sido cancelada, por lo que cada galardonado recibirá la medalla y el diploma correspondiente en su país de residencia, llevándose a cabo una ceremonia virtual de la misma en el ayuntamiento de Estocolmo en presencia de un número reducido de personalidades. Por su parte en Oslo la entrega del Premio Nobel de la Paz se hará en presencia de una muy escasa audiencia en el Paraninfo de la Universidad(4).

Figura 1. La medalla del Premio Nobel donde aparece la figura de Alfred Nobel y los años de su nacimiento y defunción.
Alfred Nobel nació el 21
octubre de 1833 en Estocolmo (Suecia) y falleció el 10 de diciembre de 1896 en
San Remo (Italia) (Figura 1). Fue ingeniero e inventor, pero también
escritor y soñador. Como hemos señalado de forma repetida en nuestro anteriores
homenajes de 2017, 2018 y 2019 (1-3), de sus más de 350 inventos de
los que se tienen noticia, sobresalen algunos como el de la dinamita, que desde
su descubrimiento ha tenido una enorme importancia en el desarrollo de las vías
de comunicación. No obstante este invento también ha jugado un papel decisivo
en las guerras del pasado, originado muchas muertes. A este respecto un
periódico, confundiendo a Alfred con un hermano Ludving, publicó erróneamente
su muerte diciendo que el mercader de la muerte había muerto, noticia
que posiblemente indujo a Nobel a crear el premio de la Paz, para paliar
parcialmente el mal potencial que podía haber generado para la humanidad por el
descubrimiento de la dinamita. Alfred Nobel, posibilitó con su fortuna, la
creación de un fondo para poder premiar a aquellas personas que sobresalieran
de forma determinante en los campos de la Paz, Literatura, Fisiología o
Medicina, Física y Química y muy posteriormente en Economía(5).
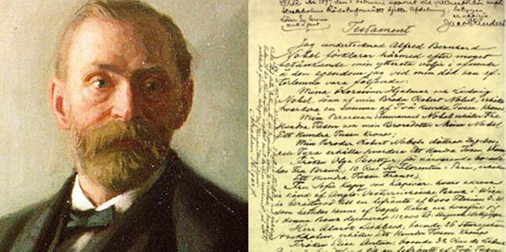
Figura 2. Alfred Nobel, inventor y fundador de los Premios Nobel junto a un fragmento de su testamento, donde se hace constar la última voluntad del inventor en relación con los Premios que llevan su nombre (7) https://www.google.es/search?newwindow=1&client=firefoxb&
dcr=0&tbm=isch&sa=1&q=Fotos+de+Alfred+Nobel+&oq
Los Premios Nobel, instituidos por el químico e inventor Alfred Nobel en su testamento, y organizados y administrados desde hace más de un siglo por la Fundación Nobel(1-3), es uno de los galardones más prestigiosos del mundo y se concede tal como figura en la página oficial del Premio For the greatest benefits to humankind” (traducción libre al castellano “Para mayor beneficio de la humanidad”(4).
Aunque existe un procedimiento de nominación y selección donde intervienen cientos de personas e instituciones de reconocido prestigio en los diferentes ámbitos de alcance de los Premios Nobel, creemos que este año, debido a la pandemia del Covid-19, el camino recorrido hasta hoy no habrá sido un camino de rosas. Es verdad que las reuniones on-line han llegado a tener enorme protagonismo, tanto en medios científicos como no científicos, de hecho la presencialidad en muchos momentos se evita. No obstante, creemos que la pandemia habrá hecho la nominación algo más compleja.
Como siempre el comienzo de todo tuvo lugar para este último Premio Nobel en septiembre del año 2019 en el que el Comité Nobel de Fisiología y Medicina (compuesto por cinco miembros elegidos por un período de tres años según los Estatutos de la Fundación Nobel, además del Secretario de la Asamblea Nobel) envió invitaciones confidenciales a personas cualificadas en el ámbito de la Fisiología y la Medicina, para que propusieran los nombres de candidatos para el Premio Nobel de Medicina, con la limitación de que no pueden auto-votarse. Entre estas personas cualificadas se han encontrado aquellas galardonadas previamente con el Premio Nobel de Medicina, los miembros del Instituto Karolinska, los miembros de la Real Academia Sueca de las Ciencias, o profesores universitarios de los países escandinavos de Fisiología y Medicina. Las propuestas de las personas cualificadas han debido ser enviadas al Comité Nobel de Medicina antes del 31 de enero del año 2020. Ya rallando información cada vez más preocupante de Wuhan (China) y de comienzos de la pandemia en Italia, el Comité durante el mes de febrero debió examinar los nombres propuestos para los Premios Nobel de Medicina. Desconocemos si el camino habrá sido similar al de otros años en el que es norma que entre los meses de marzo y mayo, el Comité Nobel de Medicina consulte con diferentes expertos los nombres de estos candidatos preliminares. A partir de aquí la situación se habrá claramente complicado, ya que normalmente el Comité Nobel de Medicina realiza un informe recabando todos los antecedentes y lo remite a la Asamblea Nobel. En dicha Asamblea Nobel se debate sobre el informe del Comité en dos reuniones distintas.
Cada octubre, la voluntad de Alfred Nobel de premiar a los que hacen verdadera ciencia (Figura 2), llega como onda expansiva a nuestras universidades y laboratorios y se hace “viral” gracias a la labor instantánea de la prensa, radio, televisión y redes sociales.
Todos los premios llevan incluida una dotación económica, que este año asciende a 10 millones de coronas suecas (prácticamente un millón de euros), a repartir en caso de que haya más de un galardonado.
En cuanto a los cuatro últimos años vemos que en 2016, recayó el premio Nobel en Yoshinori Ohsumi por sus investigaciones sobre la autofagia, un aspecto que hace pensar que en la naturaleza todo tiene un porqué y que el “reciclado”, no es sólo un proceso de limpieza, es un proceso complejo, controlado por genes, que permite la renovación y asegurar la vida y la calidad de la misma. El concepto “comerse así mismo” nacido en la década de los 60 del siglo XX, tuvo su reconocimiento 50 años más tarde.
Posteriormente, el dos de octubre de 2017 apareció en los medios la noticia “Tres americanos, descubridores del “reloj interno” del cuerpo, Nobel de Medicina 2017”. Estos autores señalaron que cada célula tenía un reloj interno autorregulado que. La comunidad científica ha constatado desde entonces la importancia de este mecanismo en la salud humana, que hace más eficaz los procesos metabólicos y homeostáticos, permitiendo que la vida, desde lo unicelular hasta nosotros mismos, sea algo más previsible y controlable. No cabe duda de que estos genes son heredables, pero su expresión y por tanto los procesos que codifican y controlan son modulados por factores epigenéticos, entre los que destaca el ambiente y la nutrición.
En 2018, el premio Nobel recae sobre un aspecto relacionado con la capacidad inmunológica del organismo y se otorga a James P. Allison y a Tasuku Honjo por su descubrimiento de la terapia contra el cáncer mediante inhibición de la regulación inmune. La aplicación de los descubrimientos de ambos de forma sinérgica ha abierto una puerta increíble, donde se ensayan ya múltiples remedios basados en la terapia inhibitoria sobre células cancerígenas conocida como "terapia de punto de control inmunitario"(6) ha cambiado las perspectivas y el pronóstico para ciertos grupos de pacientes con cáncer en estado avanzado, aunque en algunos casos debido a una hiperactividad en la respuesta inmune puede conducir a reacciones autoinmunes. Estudios clínicos recientes indican que la terapia conjunta, dirigida tanto a CTLA-4 como a PD-1, puede ser más segura como se ha encontrado en pacientes con melanoma.
Posteriormente a primeros de octubre de 2019 el Instituto Karolinska hizo público el premio for “discovery of how cells sense and adapt to oxygen availability” y lo hizo de forma conjunta para William G. Kaelin, Sir Peter Ratcliffe y Gregg L. Semenza. El secretario de la Fundación Nobel, señalaba en la presentación de los nominados al Premio de Medicina en 2019 que “los tres científicos habían logrado con sus estudios identificar la maquinaria molecular que regula la actividad de los genes en respuesta a los niveles cambiantes de oxígeno y con ello han establecido la base para entender cómo los niveles de este gas tan vital afectan el metabolismo celular y a la función fisiológica, lo que "allana el camino en el desarrollo de nuevas estrategias para combatir la anemia, el cáncer y otras muchas enfermedades. “Se trata de un mecanismo biológico fundamental que, en el cuerpo humano, regula -entre otras funciones- el desarrollo embrionario, la respiración, el metabolismo, la respiración, la inmunidad o la respuesta a la actividad física. Siendo un mecanismo tan básico, resulta interesante que esté involucrado además en múltiples enfermedades como el cáncer, el ictus cerebral, el infarto de miocardio o la anemia”, continuó, la Fundación Nobel. La investigación de estos premiados recuerda a una historia por entrega, cuyos capítulos se publicaron uno tras otro entre 1991 y 2001, como si de una serie por episodios se tratara y tiene como protagonistas principales a tres moléculas: la hormona eritropoyetina (EPO), el Factor inducible por hipoxia (HIF) y la proteína Von Hippel-Lindau (VHL).
Este año 2020, la Asamblea Nobel del Karolinska Institutet ha decidido otorgar el Premio Nobel de Fisiología o Medicina conjuntamente a Harvey J. Alter, Michael Houghton y Charles M. Rice "por el descubrimiento del virus de la hepatitis C", por su contribución decisiva a la lucha contra la hepatitis que se transmite a través transfusiones de sangre, un grave problema de salud a nivel mundial que causa cirrosis y cáncer de hígado en personas de todo el mundo. Harvey J. Alter, Michael Houghton y Charles M. Rice realizaron descubrimientos fundamentales que condujeron a la identificación de un nuevo virus, el de la hepatitis C(4).
Thomas Perlmann, secretario general del Comité Nobel y de la Asamblea Nobel, dijo en rueda de prensa que había podido ponerse en contacto con dos de los tres galardonados, los cuales al enterarse de la noticia, se mostraron "extremadamente sorprendidos, felices y casi sin palabras".
De manera muy breve y basándonos en datos bibliográficos aportados en la página del Premio Nobel(4) y en otras a las que hemos tenido acceso muy recientemente, comentaremos los principales hitos relacionados con el descubrimiento del Virus de la hepatitis C.
Según un comunicado de la Asamblea del Nobel en el Instituto Karolinska, Harvey J. Alter, nació en 1935 en Estados Unidos, recibió su título de medicina en Universidad de Rochester y trabajó en el Instituto Nacional de Salud (NIH, por sus siglas en inglés). Michael Houghton, nació en Reino Unido en 1949, recibió su doctorado en el King's College de Londres y actualmente preside la investigación de excelencia en virología en Canadá. Por su parte Charles M. Rice, nació en 1952 en Estados Unidos y recibió su título de doctorado del Instituto de Tecnología de California y está trabajando en la Universidad Rockefeller en Nueva York.

Thomas Perlmann secretario del Comité Nobel, junto al atril, anuncia los ganadores del Premio Nobel de Medicina 2020 (fotografía de Wei Xuechao/Xinhua)
Según ha destacado la Academia sueca durante la ceremonia de anuncio de los laureados, el descubrimiento de este trío estadounidense-británico-estadounidense “ha salvado millones de vidas” y “sus contribuciones han sido decisivas para combatir la hepatitis transmitida por la sangre, una enorme amenaza de salud global que causa cirrosis y cáncer de hígado en todo el planeta”.
El descubrimiento de este virus ha permitido desarrollar tests sanguíneos muy sensibles que permiten detectar la mayoría de muestras de sangre infectadas por el virus y evitar así la trasmisión de la infección. También ha hecho posible desarrollar fármacos antivirales que “por primera vez en la historia permiten que la enfermedad se cure, lo que abre la puerta a poder erradicar el virus de la hepatitis C del planeta”, en palabras de la Academia sueca.
Cinco son los virus que actualmente se conocen pueden causar hepatitis. De ellos el B y el C causan inflamación crónica del hígado. El virus de la hepatitis A se transmite principalmente a través de agua o de comida contaminada y causa una infección relativamente leve que se resuelve sin medicación en unas dos semanas y confiere inmunidad de por vida. Sin embargo la sangre y otros fluidos corporales son la vía fundamental de transmisión del virus de la hepatitis B, el cual puede producir una enfermedad hepática mucho más grave, con inflamación crónica y derivar en cirrosis y cáncer hepático. Es por ello que hasta finales de los años 70 del siglo pasado, el riesgo de contaminación del virus de la hepatitis por una transfusión era enorme, y en términos de la Academia sueca “una ruleta rusa”. A finales de los años 70, Harvey J Alter logró identificar una nueva hepatitis que llamó “hepatitis no-A, no-B. Dicha enfermedad se producía al transfundir sangre de pacientes infectados a chimpancés, siendo el aspecto patológico la inflamación hepática que no remitía sin tratamiento como la A o con los tratamientos usuales empleados en la hepatitis B.
Por su parte Michael Houghton logró secuenciar al virus y descubrió que se trataba de un virus de tipo flavivirus, al que denominó virus de la hepatitis C.
La importancia de tal descubrimiento llevó a Charles M Rice, especialista en virus, en la Universidad de Rockefeller en Nueva York (USA) a demostrar que ese flavivirus era efectivamente el causante de algunas hepatitis no–B transmitidas por transfusiones sanguíneas. Rice logró que los chimpancés a los que se había inyectado secuencias nucleotídicas específicas del virus desarrollaran la hepatitis C.
Una visión personal sobre el camino del Nobel concedido a la Hepatitis C
El Nobel, con su reconocimiento a la excelencia empuja a leer y a animar a nuestros compañeros y discípulos a que conozcan algo más sobre la noticia y su importancia científica. Pero también es importante recordar e insistir que en el camino del Nobel nada es fácil, ya que muchas actividades de años terminan en fracaso, donde la búsqueda de objetivos estrictamente prácticos generará una enorme cantidad de actividades aparentemente inútiles o consideradas “inútiles” por no ser rentables, y que el tiempo el azar, o la codicia las pone finalmente en manos afortunadas que saben hacer “útil” lo aparentemente “inútil”.
Este Premio, rodeado de anécdotas, de pequeñas o grandes errores, injusticias o anacronismos, es cada año un soplo de esperanza para muchos. No obstante, es paradójico, como nos dice Flexner(8), que en un mundo saturado de odios irracionales que amenazan a la propia civilización, algunos hombres y mujeres se alejen de esta tormenta venenosa y se entreguen a la extensión del conocimiento, al alivio de los que sufren, a la cura de las enfermedades. Corren tiempos donde se miden los descubrimientos solo por su utilidad, atando la aventura humana del saber a una conveniencia sin dejar liberar el espíritu. Wilhelm von Waldeyer en sus “Recuerdos” [citado por Flexner(8)] refiere que entre sus estudiantes se encontraba un joven pequeño, discreto y autosuficiente de 17 años llamado Paul Ehrlich que en la asignatura de Anatomía le gustaba “jugar”, “probar” tiñendo. El propio Wilhem comentaba que la idea de utilidad nunca cruzaba por la mente de Ehrlich, era interés, curiosidad, sentido profundo de saber, motilidad puramente científica, no utilitaria. Sin embargo la ciencia se benefició de que los experimentos de Ehrlich utilizados por Weigert, un compañero de estudios, llegaran al equipo de Koch y fueran utilizados para teñir bacterias y contribuir a reconocerlas y diferenciarlas. El propio Ehrlich desarrolló la técnica de tinción de frotis sanguíneos que sirve para estudiar la morfología de los leucocitos y eritrocitos y que ayuda de forma determinante al diagnóstico de muchas alteraciones hematológicas. De este modo un “juego aparentemente inútil” se convirtió en un arma de diagnóstico cotidiano en la medicina práctica de los hospitales. Ehrlich cuya curiosidad rayaba en lo especulativo, se dedicó posteriormente al estudio de la sífilis hasta conseguir una solución útil, la Arsfenamina o Salvarsán, descubrimiento que le valió nada menos que el Premio Nobel de 1908(9).
Queremos insistir de nuevo que muchos descubrimientos centrales en Medicina, por ejemplo el descubrimiento por Banting de la insulina, el de Minot y Whipple de la bondad del extracto de hígado en el tratamiento de la anemia perniciosa, tuvieron su origen en multitud de conocimientos inútiles que habían acumulado muchos estudios de científicos “puros” realizados solo por el placer de probar, y que por suerte los escogidos (no sin esfuerzo) pensaron que había llegado el momento de plantear su utilidad(8).
Pero no es nuestra idea en este homenaje de restar ni un ápice al mérito de los galardonados, por ello debemos recordar historias pasadas de los Premios Nobel ilumina nuestro asombro actual al recordar, como la ciencia, la propia humanidad han ido evolucionando. Relacionado con el Premio Nobel de Fisiología y Medicina del 2020, debemos señalar que en la década de los años 60 del siglo XX, el investigador Baruch Blumberg descubrió que el virus no-A, no-B virus estaba detrás de un tipo de hepatitis que desarrollaban muchos pacientes tras recibir una donación de sangre. Este descubrimiento le valió el Nobel de Medicina en 1976.
Como colofón a este homenaje, señalaremos que las relaciones, aparentemente sencillas, destacadas por la Academia Nobel tienen en la actualidad importantes implicaciones farmacológicas no sólo bajo el punto de vista de la cirrosis, del cáncer, sino de otras afecciones donde los cambios en el fisiologismo hepático tiene auténtico protagonismo(10).
La hepatitis, o inflamación del hígado, ha sido durante mucho tiempo parte de la historia de la humanidad. Lamentablemente, los síntomas son comunes en muchos individuos: dolor abdominal, cansancio, ictericia y, en muchos casos graves, insuficiencia hepática y muerte. La historia de la hepatitis C desde el descubrimiento hasta su curación se parece a la trama de una novela de misterio. Comienza con un desconcertante quién lo hizo, seguido de una larga búsqueda del sospechoso y, finalmente, esfuerzos rigurosos para someter al culpable. Muchos de estos esfuerzos fueron encabezados por el National Institute of Diabetes and Digestive and Kidney (NIDDK) y, aunque la historia no está acabada, los resultados de la batalla contra la hepatitis C puede definirse de muy exitosa en la investigación científica(10).
Un culpable desconocido
No fue hasta el siglo XX cuando se descubrió que la mayoría de los casos de hepatitis eran causados por virus que infectan las células del hígado. En la década de los 60 y principios de los 70 del siglo pasado, se consideró que la hepatitis viral representaba dos enfermedades distintas bajo el punto clínico y epidemiológico: hepatitis infecciosa y hepatitis sérica(11). La hepatitis infecciosa o hepatitis A, se caracterizaba por un período de incubación corto (1 a 3 semanas), transmisión fecal-oral, un alto grado de contagio y por ser una enfermedad aguda autolimitada que podría prolongarse y ser grave (e incluso fatal) pero que no resultaba en hepatitis crónica o cirrosis. La “hepatitis A” se transmitía por contacto de persona a persona o mediante agua o alimentos contaminados, tenía un período de incubación corto y resultó en una enfermedad aguda (temporal pero grave).
Por su parte la hepatitis sérica, o hepatitis B, presentaba un período de incubación más largo (1-3 meses), era de transmisión parenteral o sexual, de bajo grado de contagio y definida por ser una enfermedad aguda, generalmente autolimitada, pero que podía ser grave o fatal, pudiendo resultar en infección crónica, hepatitis crónica e incluso cirrosis.
Esta dualidad fue apoyada por estudios de transmisión en humanos(11) y por el descubrimiento de que el antígeno Australia era parte integrante del virus de la hepatitis B (VHB)(12-14) . El desarrollo de pruebas sensibles para el antígeno Australia, posteriormente denominadol HBsAg (antígeno de superficie de la hepatitis B), proporcionó un medio de diagnóstico y detección que podría aplicarse a las donaciones de sangre para prevenir la hepatitis postransfusional(15). Dado que muchos casos de hepatitis parecían provenir de transfusiones de sangre, la identificación de los virus, en particular el agente sanguíneo que causaba la hepatitis B, se volvió imperativa. Si se conocía el virus, se podía examinar el suministro de sangre para prevenir la propagación de la enfermedad. El cribado de HBsAg en las sangres de donantes, sin embargo, condujo a una disminución de sólo el 25-50% en hepatitis postransfusional(16). Los casos residuales se consideraron debidos a hepatitis A o hepatitis B que no habían sido detectados por los ensayos serológicos disponibles en ese momento.
Sin embargo, a mediados de la década de 1970, los investigadores de los NIH en la Sección de Hepatitis del Laboratorio de Enfermedades Infecciosas del Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID) habían identificado el virus de la hepatitis A y, en colaboración con el Centro Clínico de los NIH División de Medicina Transfusional, demostraron que los casos restantes de hepatitis no eran ni hepatitis A ni hepatitis B, por lo que había muchas posibilidades de que se tratara de un tercer virus. Al igual que la hepatitis B, esta enfermedad recién identificada podría contraerse a través de la sangre infectada y podría provocar una infección crónica y cirrosis hepática. Sin embargo, la probabilidad de enfermedad crónica en adultos era mucho mayor que con la hepatitis B. Además, a diferencia de la hepatitis B, las personas con esta enfermedad rara vez experimentan síntomas agudos, lo que podría significar que la enfermedad podría pasar a un estado crónico antes de que una persona presentara síntomas signos de que incluso estaba infectado. Durante los siguientes 15 años, no se identificó al “sigiloso” culpable de esta enfermedad, por lo que la enfermedad se denominó simplemente hepatitis no-A, no-B.
La hepatitis no-A y no-B
Incluso sin un agente identificable, las características clínicas y epidemiológicas de la hepatitis no-A, no-B estaban bien definidas(17). La enfermedad se debía a un agente transmisible, probablemente un virus, de 40-60 nm de tamaño, con envoltura, sensible al calor y que sufría inactivación por el cloroformo. La enfermedad se transmitía por sangre e inyecciones, consumo de drogas, pero rara vez por exposición sexual o materno infantil. La infección aguda tendía a ser leve y asintomática, pero también podía causar ictericia y hepatitis severa. También conviene destacar que la hepatitis no-A, no-B aguda conducía frecuentemente a una hepatitis persistente y crónica, y en algunos casos producía cirrosis y carcinoma hepatocelular.
Posteriormente se demostró que la infección aguda por el virus no-A, no-B provocó una infección persistente en al menos el 75% de los casos, convirtiéndose en el mundo occidental en la causa más común de hepatitis crónica, cirrosis y carcinoma hepatocelular.
Mientras los científicos buscaban al misterioso “nuevo agente”, sus esfuerzos también se concentraron en el tratamiento. Los primeros medicamentos que se probaron fueron aquellos que habían demostrado ser eficaces contra una amplia gama de virus. En particular dado que los pacientes con hepatitis B respondían con bastante éxito al interferón alfa (IFNa), se probó como una herramienta terapéutica contra el virus no identificado que causaba la hepatitis no-A y no-B. El nombre de interferón, sustancia, producida por las células del sistema inmune, proviene del concepto de "interferir" en la replicación del virus, protegiendo a las células contra la infección.
En 1984, los científicos del Programa de Investigación Intramural del NIDDK dirigieron un estudio piloto de interferón en 10 pacientes en el Centro Clínico de los NIH en Bethesda, Maryland(18). Los pacientes recibieron dosis diarias durante 16 semanas y se controló la salud de su hígado analizando su sangre para detectar los cambios en la enzima alanina-amino transferasa (ALT), un marcador de daño hepático. Los resultados del ensayo fueron contundentes: la mayoría de los pacientes mostraron mejorías indudables en el hígado después de un mes de tratamiento. Los pacientes recayeron cuando se interrumpió el tratamiento con interferón después de 4 meses; sin embargo, una vez que se reinició el tratamiento, la salud de su hígado volvió a mejorar y se mantuvo normal incluso después de que la dosis se redujo gradualmente y luego se detuvo después de un año completo [para más detalles consultar la revisión de Pawlotsky y col.(19)]. Algunos de los pacientes tuvieron solo respuestas mínimas a la terapia con interferón, otros respondieron inicialmente para recaer después. No obstante, la mitad de los pacientes en el ensayo no mostraron signos de infección hepática en los seguimientos que finalmente se extendieron de 10 a 25 años. Estos fueron los primeros pacientes que se curaron de la enfermedad que posteriormente se conocería como hepatitis C.
A pesar de estos beneficios, la disparidad de resultados derivados de otros estudios moderó las expectativas con el interferón. En general los pacientes que lograban una adecuada tasa de respuesta virológica sostenida (RVS) no tenían virus detectable durante al menos 24 semanas después de suspender el tratamiento, lo que significaba que había una probabilidad muy alta de que el tratamiento hubiera tenido éxito y el paciente no mostrara recidivas.
El tratamiento con interferón solo arrojó típicamente tasas de RVS de menos del 20 por ciento. Sin embargo, la combinación de interferón con otros medicamentos antivirales resultó prometedora. Uno de estos medicamentos, la ribavirina, había sido probado por primera vez por investigadores del NIDDK como una terapia independiente, pero solo habían tenido un efecto modesto y temporal en los niveles de virus. Sin embargo, estudios posteriores mostraron que una combinación de interferón y ribavirina era superior a solo interferón, mostrando tasas de RVS del 30 al 40 por ciento(20,21). Otra mejora se produjo cuando los científicos modificaron químicamente el interferón para incrementar su vida media y lograr que durara más tiempo en el cuerpo. Con tasas de RVS del 55 por ciento, este interferón modificado con polietilenglicol (peginterferón), combinado con ribavirina, se convirtió en el estándar de tratamiento para los pacientes con hepatitis C(22,23).
Los resultados de estos estudios también mostraron que se necesitaba más investigación. Si bien la terapia basada en interferón fue generalmente exitosa para más de la mitad de los pacientes, generalmente estuvo acompañada de efectos secundarios como fiebre, fatiga, dolores musculares y depresión que a menudo limitaban la dosis y la duración de los tratamientos. Sin embargo, estos ensayos iniciales proporcionaron información importante sobre cómo el virus respondía (o resistía) a la terapia y proporcionaron pistas importantes sobre la biología y la resistencia del virus, que resultó útil a la hora de diseñar terapias basadas en tratamientos más eficaces.
El descubrimiento del virus de la hepatitis C
El virus de la hepatitis no-A, no-B fue identificado en 1989 por científicos de la empresa de biotecnología de California llamada Chiron que colaboraban con investigadores de los Centros para el Control y la Prevención de Enfermedades (CDC). La investigación confirmó que se trataba de un nuevo virus, al que se le llamó oficialmente virus de la hepatitis C o VHC. Este avance histórico en la medicina permitió el desarrollo de pruebas para detectar el VHC, que se aplicaron rápidamente para controlar las donaciones de sangre y evitar la presencia e infección por VHC al recibir una transfusión sanguínea. La identificación del VHC también condujo a estudios adicionales, realizados por investigadores financiados por el NIAID, NIDDK y otros, para determinar su estructura molecular. Se trataba de un virus ARN, de polaridad negativa, formado por una cadena simple, circular y corta, con una cápside icosaédrica y con envoltura que correspondía a la envoltura del virus de la hepepatitis B o HBsAg (por lo que requería de la infección con este virus para su desarrollo). Esto fue crucial para el diseño de medicamentos que interactuarían específicamente con componentes del virus e inhibirían su replicación. La identificación del virus también permitió un diagnóstico más preciso y una mejor percepción de su prevalencia; de hecho, finalmente se determinó que el VHC era la causa más común de hepatitis crónica, cirrosis y cáncer de hígado en el mundo occidental(19).
La aplicación de nuevas pruebas directas para la presencia de VHC mostró que la terapia con interferón reducía el nivel de virus en la sangre y lo que era más importante, los pacientes que tuvieron una respuesta clínica al tratamiento y no recayeron se volvieron también negativos para el VHC y se curaron de su infección viral crónica. Las pruebas de ARN del VHC en sangre fueron clave para el progreso futuro del tratamiento, porque demostraron que una pérdida sostenida del ARN del VHC durante 12 semanas después de suspender el tratamiento era un criterio de valoración fiable de la eficacia del mismo. La evaluación del RVS se convirtió en punto obligado de referencia para los ensayos clínicos de nuevos tratamientos. También dio lugar que para que se produjera la aceptación de una nueva terapia, las tasas de RVS debían ser mayores que las conseguidas con la combinación de peginterferón y ribavirina.
El estudio de la composición genética del VHC reveló que el virus tiene varios genotipos o variedades genéticas, y estos determinan la eficacia con la que el virus responde a la terapia. Una contribución importante fue el descubrimiento, por medios de estudios de asociación de genoma completo (GWAS), de la existencia de un solo polimorfismo de nucleótidos ubicados “aguas arriba” del gen de la interleucina-28B (IL28B) fuertemente asociado con la probabilidad de una RVS después de la terapia con PegIFN-a y ribavirina. También se encontró que el genotipo 1 era más común pero más resistente a la terapia con interferón que otros genotipos(24). El polimorfismo del nucleótido rs12979860 fue un buen predictor de RVS en pacientes infectados con el genotipo 1 que recibían esta terapia(24). Por su parte el genotipo IL28B estaba fuertemente asociado con el origen étnico y era un marcador genético de la capacidad de respuesta al IFN del paciente(24). Más recientemente, otro polimorfismo se identificó en la misma región, que afectaba la codificación de una nueva proteína, cuyo nombre era IFN-k4, y también al aclaramiento espontáneo del VHC con la respuesta a la terapia basada en IFN-α(25). Sin embargo, a nivel individual, se lograba una mejor predicción mediante el seguimiento de cinética viral en tratamiento. Es decir, la identificación de diferentes genotipos significó que los investigadores pudieron predecir y adaptar mejor las terapias, y proporcionó una explicación de por qué algunos participantes de ensayos clínicos tuvieron mejores resultados con peginterferón que otros(24,25). Otra consecuencia importante de la identificación del VHC fue que se logró analizar los componentes moleculares del virus y determinar cuáles podrían ser objetivos ideales para los medicamentos. Estos objetivos potenciales incluían la polimerasa del VHC, crucial para la replicación del material genético del virus; una enzima llamada proteasa que utiliza el virus para procesar sus componentes antes del ensamblaje; y una proteína llamada NS5A, que parece tener varias funciones importantes en la replicación del virus, incluida la regulación de la respuesta celular al interferón(10).
Mientras que los científicos trabajaban para caracterizar el VHC, también avanzaban en su tratamiento. Un gran paso hacia el diseño de fármacos se produjo en 2005, cuando tres grupos diferentes de investigadores, incluidos los investigadores del NIDDK, hicieron en el laboratorio crecer el virus en células. Esto permitió conocer el ciclo de vida del VHC y la identificación de componentes virales esenciales.
Posteriormente se desarrollaron terapias diseñadas específicamente para bloquear la replicación del VHC dirigiéndose directamente a partes del virus. Si bien las terapias ampliamente antivirales como el interferón y la ribavirina fueron algo efectivas, los efectos secundarios hicieron que los tratamientos fueran difíciles de tolerar. Por tanto, todo se orientó posteriormente a diseñar medicamentos que atacaran específicamente al VHC y a las células infectadas por el virus, minimizando en gran medida el daño a otras partes del cuerpo.
Cero interferon en el virus de la hepatitis C
La era de los antivirales de acción directa (AAD) que se dirigen específicamente al VHC comenzó en 2011 con la aprobación de la Administración de Drogas y Alimentos (FDA) de los EE. UU. de los primeros inhibidores de la proteasa(10,19). Estos medicamentos, telaprevir y boceprevir, junto a otros medicamentos similares aprobados posteriormente, se dirigieron a la proteasa del VHC que es fundamental para la replicación viral. Cuando se usaron junto con peginterferón y ribavirina, los inhibidores de la proteasa produjeron tasas de RVS de hasta el 75 por ciento(26). Sin embargo, esta triple terapia estuvo acompañada de efectos secundarios adicionales a los ya presentes con peginterferón y ribavirina. No obstante, el éxito de los inhibidores específicos de proteasa del VHC demostró que el virus presentaba vulnerabilidad.
Durante los siguientes años se desarrollaron y probaron más medicamentos nuevos contra el VHC. Estos nuevos fármacos incluían sofosbuvir y dasabuvir, que interferían con la actividad de la polimerasa del VHC(19). Los miembros de una segunda clase de medicamentos, ledipasvir y daclatasvir, se dirigieron a la región NS5A del virus, interaccionando con una proteína estructural crítica para la replicación viral. Muchos de estos medicamentos se probaron inicialmente junto con peginterferón y ribavirina, o en combinación con un inhibidor de proteasa. Generalmente, los resultados dieron tasas de RVS de al menos el 80 por ciento.
Con el éxito de las terapias ADD se hizo evidente que cuando varias fármacos se usaban en combinación, el interferón ya no era necesario, evitando con ello los muchos efectos secundarios que se producían con la terapia basada en peginterferón. Estos regímenes totalmente orales también abrieron la posibilidad de tratamiento en personas en las que no se podía administrar peginterferón de forma segura. Quizás la combinación de ADD más exitosa fue la de sofosbuvir y ledipasvir; con estos dos medicamentos, las tasas de RVS superaron el 99 por ciento(27-29).
No nos cabe duda de que en estas líneas no podemos hacer un análisis más pormenorizado del actual tratamiento de la hepatitis C, y que aumentar su extensión borraría el auténtico enfoque de esta editorial. Por ello creemos que algún especialista en farmacia clínica podría desarrollar con mucho mejor detalle las bases del tratamiento actual de la Hepatitis C en España y en otros países.
Hay que señalar que los medicamentos actuales son muy prometedores, pero los costos de los tratamientos ADD aprobados por la FDA más exitosos son extremadamente altos, lo que representa un obstáculo significativo para muchas personas con la enfermedad.
La vacuna. El futuro de la terapia contra la hepatitis C
Con tasas tan elevadas de éxito con los tratamientos actuales, podría parecer que la historia de la hepatitis C está prácticamente escrita, pero realmente aún no se ha terminado. Una vacuna contra la hepatitis C haría que la prevalencia de la enfermedad y la morbi-mortalidad asociadas cayeran en picado, pero los esfuerzos para producir una vacuna, aunque todavía están en marcha, aún no han tenido éxito. Si bien las hepatitis A y B tienen vacunas, el virus de la hepatitis C es más variable que cualquiera de estos dos virus, lo que, junto con otros factores, complica los esfuerzos del desarrollo de vacunas.
Referencias
1. Sánchez-Muniz FJ, Culebras JM, Vicente-Vacas L. In the month of the Nobel Prize Awards, we pay tribute to Alfred Nobel and to the recipients of the 2017 Prize in Physiology and Medicine. JONNPR 2017; 2(11): 577-580.
2. Sánchez-Muniz FJ, Culebras JM, Vicente-Vacas L. In the month of the Nobel Prize Awards, we pay tribute to Alfred Nobel and to the recipients of the 2018 Prize in Physiology and Medicine. JONNPR 2018; 3(11): 857-665.
3. Sánchez-Muniz FJ, Culebras JM, Vicente-Vacas L. We pay tribute to Alfred Nobel and to the recipients of the 2019 Prize in Physiology and Medicine. JONNPR. 2020;5(3):236-45. DOI: 10.19230/jonnpr.3451
4. Premio Nobel de Medicina 2020: Página Oficial. https://www.nobelprizemedicine.org/the-nobel-prize-in-physiology-or-medicine-2020/
5. Rincón del vago https://www.rincondelvago.com/informacion/premios-nobel/
6. Nobel de Medicina por investigación celular - BBC News Mundowww.bbc.com › 2009/10 › 091005_nobel_medicina_jp
8. Flexner A. La utilidad de los conocimientos útiles. En: La utilidad de lo inútil. Manifiesto. Ordina N (ed.). Acantilado, Barcelona, 2013; pp153-171.
9. Ehrlich P. www.historiadelamedicina.org
10. Research Update, june 9, 2016. Story of discovery: hepatitis C: from non-A, non-B hepatitis to cure.
11. Krugman S, Giles JP, Hammond J. Infectious hepatitis. Evidence for two distinctive clinical, epidemiological, and immunological types of infection. JAMA 1967;200:365–373.
12. Blumberg BS, Alter HJ, Visnich S. A ‘‘new’’ antigen in leukemia sera. JAMA 1965;191:541–546.
13. Krugman S, Giles JP. Viral hepatitis. New light on an old disease. JAMA 1970;212:1019–1029.
14. Prince AM. An antigen detected in the blood during the incubation period of serum hepatitis. Proc Natl Acad Sci U S A 1968;60:814–821.
15. Gocke DJ. A prospective study of posttransfusion hepatitis. The role of Australia antigen. JAMA 1972;219:1165–1170.
16. Alter HJ, Holland PV, Purcell RH, Lander JJ, Feinstone SM, Morrow AG, et al. Posttransfusion hepatitis after exclusion of commercial and hepatitis-B antigen-positive donors. Ann Intern Med 1972;77:691–699.
17. Dienstag JL. Non-A, non-B hepatitis. I. Recognition, epidemiology, and clinical features. Gastroenterology 1983;85:439–462.
18. Hoofnagle JH, Mullen KD, Jones DB, Rustgi V, Di Bisceglie A, Peters M, et al. Treatment of chronic non-A, non-B hepatitis with recombinant human alpha interferon. A preliminary report. N Engl J Med 1986;315:1575–1578.
19. Pawlotsky JM, Feld JJ, Zeuzem S, Hoofnagle JH. From non-A, non-B hepatitis to hepatitis C virus cure. J Hepatol 2015; 62 j:S87–S99.
20. McHutchison JG, Gordon SC, Schiff ER, Shiffman ML, Lee WM, Rustgi VK, et al. Interferon alfa-2b alone or in combination with ribavirin as initial treatment for chronic hepatitis C. N Engl J Med 1998;339:1485–1492.
21. Poynard T, Marcellin P, Lee SS, Niederau C, Minuk GS, Ideo G, et al. Randomised trial of interferon alpha-2b plus ribavirin for 48 weeks or for 24 weeks versus interferon alpha-2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. Lancet 1998;352: 1426–1432.
22. Neumann AU, Lam NP, Dahari H, Gretch DR, Wiley TE, Layden TJ, et al. Hepatitis C viral dynamics in vivo and the antiviral efficacy of interferon-alpha therapy. Science 1998;282:103–107.
23. Herrmann E, Lee JH, Marinos G, Modi M, Zeuzem S. Effect of ribavirin on hepatitis C viral kinetics in patients treated with pegylated interferon. Hepatology 2003;37:1351–1358.
24. Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, et al. Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance. Nature 2009;461:399–401.
25. Prokunina-Olsson L, Muchmore B, Tang W, Pfeiffer RM, Park H, Dickensheets H, et al. A variant upstream of IFNL3 (IL28B) creating a new interferon gene IFNL4 is associated with impaired clearance of hepatitis C virus. Nat Genet 2013;45:164–171.
26. Sulkowski MS, Gardiner DF, Rodriguez-Torres M, Reddy KR, Hassanein T, Jacobson I, et al. Daclatasvir plus sofosbuvir for previously treated or untreated chronic HCV infection. N Engl J Med 2014;370:211–221.
27. Bourlière M, Sulkowski MS, Omata M, Zeuzem S, Feld JJ, Lawitz E, et al. An integrated safety and efficacy analysis of >500 patients with compensated cirrhosis treated with ledipasvir/sofosbuvir with or without ribavirin. Hepatology 2014;60:239A.
28. Flamm SL, Everson GT, Charlton M, Denning JM, Arterburn S, Brandt-Sarif T, et al. Ledipasvir/sofosbuvir with ribavirin for the treatment of HCV in patients with decompensated cirrhosis: preliminary results of a prospective, multicenter study. Hepatology 2014;60:320A.
29. Reddy RK, Everson GT, Flamm SL, Denning JM, Arterburn S, Brandt-Sarif T, et al. Ledipasvir/sofosbuvir with ribavirin for the treatment of HCV in patients with post-transplant recurrence: preliminary results of a prospective, multicenter study. Hepatology 2014;60:200A.