REVISIÓN
Acerca de la enfermedad celiaca. Breve historia de la celiaquía
Brief history of Coeliac disease
Ángeles Rodríguez Montealegre, Paloma Celada, Sara Bastida, Francisco J Sánchez-Muniz
Departamento de Nutrición y Ciencia de los Alimentos. Facultad de Farmacia. Universidad Complutense de Madrid. Madrid. España
* Autor para correspondencia.
Los artículos publicados en esta revista se distribuyen con la licencia:
Articles published in this journal are licensed with a:
Creative Commons Attribution 4.0.
https://creativecommons.org/licenses/by-nc-nd/4.0/
La revista no cobra tasas por el envío de trabajos,
Resumen
En este trabajo sobre enfermedad celiaca, los autores se centran fundamentalmente en los aspectos históricos más relevantes que han ido pautando el conocimiento sobre la enfermedad celiaca. A medida que se han ido conociendo más detalles de la enfermedad a través de sus síntomas se hizo un perfil más riguroso de esta patología. Así, primero se la consideró una indigestión crónica sin relación con el tipo de alimento ingerido, luego se comprobó que se basaba en una intolerancia a la gliadina y a otras proteínas similares para conocer, más tarde que es una enfermedad autoinmune. Se revisan las contribuciones de personajes tan importantes como Areteo de Capadocia, Soriano, Gee, Herter, Dicke, Anderson o Marsh que con sus contribuciones e investigaciones han ayudado de forma indiscutible al conocimiento de los aspectos centrales de la enfermedad celiaca. Este artículo no quiere obviar el trabajo de médicos y científicos españoles entre los que destacan Santiago Cavengt, Manuel Suarez Perdiguero, Ángel Ballabriga, Isabel Polanco ni tampoco la labor ingente de las sociedades de celiacos internacionales y nacionales y del Ministerio de Sanidad y Consumo.
Palabras clave
Historia; enfermedad celiaca; hitos destacados
Abstract
In this work on celiac disease, the authors focus mainly on the most relevant historical aspects that have been patterning knowledge on celiac disease. Once more details of the disease through their symptoms have been known, a more rigorous profile of this pathology was made. Thus, the Celiac Diseases first was considered a chronic indigestion without relation to the type of food ingested, then it was found that it was based on an intolerance to gliadin and other similar proteins, later that it is an autoimmune disease. The important contributions of Areteo, Soriano, Gee, Herter, Dicke, Anderson, Marsh are reviewed and their contributions and research have helped indisputably the knowledge of the central aspects of the Celiac Disease. This paper does not want to obviate the work of Spanish physicians and researcher as Santiago Cavengt, Ángel Ballabriga, Manuel Suárez Perdiguero, Isabel Polanco nor the work of the international and national Celiacs societies and the Spanish “Ministry of Salud y Consumo”.
Keywords
History; coeliac disease; highlights
Introducción
La enfermedad celíaca (EC) o celiaquía es una patología crónica e autoinmune que afecta múltiples órganos, dañando primero el intestino para lesionar posteriormente otras zonas del cuerpo(1,2), especialmente en individuos con una predisposición genética a padecer esta enfermedad. La gravedad de esta patología es dependiente de la edad del paciente y de su situación fisiopatológica(3,4).
La EC se debe a una intolerancia permanente a algunas proteínas que se encuentran en los cereales, principalmente la gliadina y otras proteínas afines, presentes en cereales como el trigo avena, cebada y centeno o cualquiera de sus variedades e híbridos (escanda, espelta, kamut y triticale, entre otros) y productos derivados(5-7). Esta intolerancia genera la atrofia severa de las vellosidades intestinales que, a su vez, produce una grave mala absorción de los nutrientes en el intestino(4).
Pero la EC no solo es una intolerancia alimentaria, es una enfermedad sistémica(8,9). El gluten provoca en los pacientes una respuesta inmunológica anormal generando autoanticuerpos(10,11) que pueden atacar a todo el organismo, no solo al intestino(1,2). Cuando la EC no es tratada adecuadamente puede derivar en complicaciones graves como cáncer, trastornos neurológicos y psiquiátricos (denominados neurogluten), enfermedades cardiovasculares y osteoporosis(4,12-14). No obstante, hay casos en los que como en la enfermedad celíaca refractaria, no se consiguen mejorías con el tratamiento con dieta y, además, en situaciones, particularmente en los niños, se puede dar la llamada ‘crisis celíaca’ que aparece súbitamente y que suele ser mortal(14).
Es la enfermedad crónica intestinal que con más frecuencia aparece en los niños, siendo en la actualidad entre un 1/100-1/150 de la población total. Si bien es verdad que su incidencia ha aumentado en los últimos años, este aumento puede explicarse por el uso de métodos diagnósticos más sensibles que detectan la enfermedad en estadios muy tempranos y/o en fases asintomáticas(15). En cualquier caso, un diagnóstico precoz y un tratamiento correcto son imprescindibles para evitar que la enfermedad produzca efectos graves sobre el organismo.
Breve revisión histórica
En la historia de la enfermedad pueden considerarse diferentes fases delimitadas por avances en el diagnóstico y en el conocimiento etiopatogénico de la misma(12).
Areteo de Capadocia (Figura 1), médico griego del siglo I d.C. que vivió durante el reinado de Nerón o Vespasiano, es el primero en describir un caso de EC en su tratado “Sobre las causas y los síntomas de las enfermedades” (editado y traducido por Francis Adams en 1856)(16). Por lo tanto, la primera mención a la celiaquía se da en el siglo I d.C.

Figura 1. Areteo de Capadocia (Siglo I d.C.)
Areteo en el capítulo ‘Diatesis celíaca’ de aquel tratado describe la diarrea grasa o esteatorrea como uno de los síntomas de la enfermedad que se da tanto en niños como en adultos, además de otros elementos que suelen acompañarla, como la pérdida de peso y la diarrea crónica reincidente. En otro capítulo del mismo tratado se emplea el término ‘celíaco’ para calificar a los enfermos que padecen este mal: “si el estómago no retiene los alimentos y pasan a través de él sin ser digeridos, y nada es asimilado por el organismo, denominamos a tales personas como celíacas”. Exactamente el vocablo utilizado es la palabra griega koliakos que quiere decir ‘aquellos que sufren del intestino’.
Areteo también menciona en su tratado, cuando se refiere a la celiaquía, que “el pan es raramente adecuado para proporcionar energía (a los niños celíacos)”(17). De esta observación se puede colegir que el médico griego ya sospechaba de los efectos adversos del pan sobre los niños intuyendo en gran parte la causa del problema celíaco.
Que Areteo de Capadocia sea el primer médico que hace referencia a la enfermedad celiaca, no parece una casualidad, sino un hecho basado en la probabilística, ya que este médico reside al este de Turquía en un territorio del Oriente Próximo conocido como “Media Luna Fértil” o “Creciente fértil” (Figura 2), ubicado entre los ríos Éufrates y Tigris y el Nilo. En esa zona tiene lugar una gran revolución en la alimentación, condicionada por el cultivo de cereales, que implica un incremento muy marcado en el consumo de granos que contienen gluten, creando las condiciones para la aparición de enfermedades relacionadas con la exposición a sus proteínas.
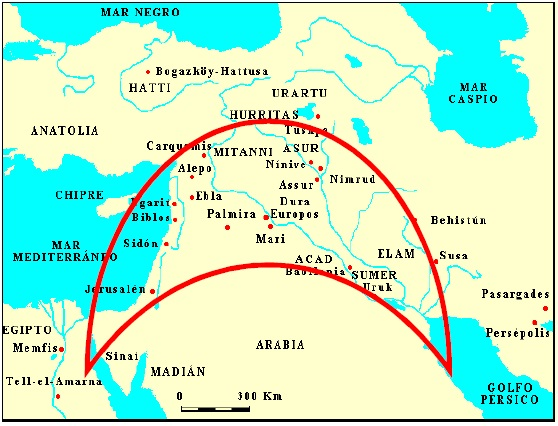
Figura 2. Territorio de la Media Luna Fértil. En esta zona del Oriente Próximo, bien
abastecida de agua dulce tuvo lugar, a partir del Neolítico, un desarrollo exponencial de
la agricultura. Creado a partir de http://www.proel.org/img/alfabetos/medorien.gif
Mucho más tarde, en los albores del siglo XVII, el médico turolense Jerónimo Soriano en su libro Método y orden de curar las enfermedades de los niños (Figura 3) afirma, en el capítulo De la curación de las cámaras, que existen diferentes tipos de diarreas (llamadas cámaras en ese tratado). Unas son las celíacas, donde “lo que se vacía es con muy poca alteración o mutación”. También reseña que “De todas estas diferencias de cámaras, tratamos largo en el libro de nuestros experimentos médicos. Allí hallarán remedios maravillosos”(18).

Figura 3. Método y orden de curar las enfermedades de los niños: Tratado de Jerónimo
Soriano (Publicado en 1600).
https://www.bing.com/search?q=jeronimo+soriano&src=IE-SearchBox&FORM...
La EC aparece de nuevo en la bibliografía médica dos siglos después, cuando un médico británico, Samuel Gee (Figura 4), imparte una conferencia en Londres (Gee 1888)(19,20) donde señala: “Hay una especie de indigestión crónica que se da en personas de todas las edades, pero que tiene una tendencia especial a afectar a niños de entre uno y cinco años. Los signos de la enfermedad se producen en las heces, que son sueltas, no formadas, pero no líquidas, más voluminosas de lo que los alimentos ingeridos parecían justificar; de color pálido, como si contuvieran bilis; con aspecto de levadura y espuma, probablemente debido a la fermentación, con un hedor con frecuencia muy fuerte, puesto que los alimentos experimentan putrefacción en lugar de digestión”(20).

Figura 4. Samuel Gee (1839-1911). Tomada de
https://en.wikipedia.org/wiki/Samuel_Gee
Por lo tanto, Gee describe la celiaquía como un síndrome de mala absorción intestinal que se desencadena al ingerir algún alimento y sugiere que “si el paciente puede ser curado por completo, debe ser por medio de la dieta”. Aunque acierta al describir la EC se equivoca al recomendar que los pacientes afectados se alimenten con pan “cortado fino y bien tostado por ambos lados”.
Aunque la primera insinuación de relación entre la dermatitis herpetiforme y la enfermedad celíaca no se hace hasta 1955, es en 1884 cuando Louis Dühring describe por primera vez tal afectación cutánea, pero sin relacionarla con la celiaquía, ni separarla claramente de otras enfermedades cutáneas que cursan con ampollas(20).
También en el siglo XIX, Christian Archibald Herter (Figura 5), un pediatra norteamerican, escribe “On infantilism from Chronic Intestinal Infection”. Este médico afirma que “las grasas son mejor toleradas que los hidratos de carbono”, contribuyendo con esta observación en el avance para tratar la EC. Su aportación es tan importante que a esta enfermedad se la llega a llamar la enfermedad de Gee-Herter(21).

Figura 5. Christian Archibald Herter (1865-1910). Tomada de:
https://en.wikipedia.org/wiki/Christian_Archibald_Herter_(physician)
Sir George Frederic Still, considerado el padre de la pediatría británica, imparte en 1921 una lección magistral en el Royal College of Physicians, en la que se explaya hablando sobre los efectos perniciosos del pan en la EC. Ese mismo año esta aseveración es desarrollada por John Howland en su discurso “Prolongada intolerancia a los hidratos de carbono” impartido en la American Pediatric Society. Howland resalta la importancia de excluir/reducir los hidratos de carbono en las dietas de los niños celíacos: “Las experiencias clínicas han mostrado que, de todos los elementos de las sustancias nutritivas, los hidratos de carbono son los que deben ser rigurosamente excluidos, una vez estos ampliamente reducidos, los otros elementos son casi siempre bien aceptados teniendo en cuenta que la absorción de las grasas no es tan satisfactoria como en las personas sanas”. Asimismo, asevera que la dieta, dividida en tres fases, solo admite la ingesta de hidratos de carbonos en la última de ellas, en la que aconseja, tras observar la capacidad y reacción del intestino, añadir gradualmente los cereales. Howland recalca que el tratamiento es severo pero efectivo a largo plazo(18).
En nuestro país también hubo pediatras que observaron las anomalías digestivas que presentaban algunos de sus pacientes. Uno de los más reconocidos es Santiago Cavengt Gutiérrez (Figura 6).

Figura 6. Santiago Cavengt Gutiérrez. Retrato realizado por José Antonio Ávila.
Tomado de: https://www.bancodeimagen esmedicina.com/index.php/banco-deimagenes/
retratos/cavengt-gutierrez-santiago-4912
Este pediatra del Hospital Niño Jesús de Madrid escribe en 1922, Endocrinología Infantil; en este libro habla de “los patocativismos infantiles pluriglandulares de origen intestinal” (22). Cuatro años después Cavengt publica en la revista La Pediatría Española dos casos de enfermedad celíaca con el nombre de infantilismo digestivo. En este artículo reconoce estar al tanto de los trabajos de Gee, pero habla de conceptos nuevos como la relación de la enfermedad con el metabolismo óseo. Este pediatra español fue el primero en dar a conocer la EC en España. Su interés por esta enfermedad permanece intacto durante varias décadas pues en el año 1950 se lee una comunicación suya en una Reunión de la Sociedad de Pediatría de Madrid, cuyo título es “Consideraciones clínicas sobre la celiaquía”(23).
Posteriormente las reseñas sobre EC no son frecuentes. Tan solo resaltar que en 1935, el catedrático de Pediatría de la Facultad de Medicina de Barcelona Martínez Vargas publica en la revista La Medicina de los niños un artículo donde habla de enfermedad celíaca, recogiendo la descripción de Recalde Cuestas y Travella “la mayoría de estos niños son neurópatas, caprichosos, propensos a la cólera, a la inapetencia y a la bulimia”(18).
En 1945, otro profesor universitario y español, Manuel Suárez Perdiguero, realiza un estudio sobre 17 niños celíacos. En las exploraciones comprueba que los pacientes tienen una curva de glucemia plana cuando se realizaba por vía oral y normal por vía endovenosa. Por otra parte, las radiografías del tracto intestinal presentan un tránsito lento de la papilla en el propio intestino delgado, así como unas asas dilatadas y atónicas. Ante estas observaciones, el doctor Suárez concluye que la enfermedad se debe a una insuficiencia funcional del intestino delgado(24).
Más tarde, en 1950, el médico holandés Willem Karel Dicke (Figura 7), defiende en su tesis doctoral en la universidad de Utrecht, la importancia de eliminar de la dieta de los niños celíacos el trigo, el centeno y la harina de avena, hecho que implica un gran avance en lo referente a una Dieta sin gluten en el tratamiento de la EC.
Figura 7. Willem Karel Dicke (1905-1962).
https://www.google.com/search?q=Willem+Karel+Dicke+fotos+de+libre+acceso&clien
t=firefox-bab&
tbm=isch&tbo=u&source=univ&sa=X&ved=2ahUKEwj42cjBp5_eAhWj4YUKHc
yOA-YQ7Al6BAgGEA0&biw=1920&bih=926
Dicke observa que la tasa de mortalidad infantil entre los celíacos antes de la Segunda Guerra Mundial era más elevada que durante la misma (pasó del 30-35% a casi el 0%) y lo asocia a que a los niños durante esa guerra se les suministraba en el hospital, diferentes papillas de vegetales, pero raramente con harina de trigo(20). De estos datos intuye que la harina de trigo puede estar relacionada con esa disminución de mortalidad. Basándose en esta intuición realiza un ensayo clínico en un número reducido de niños para demostrar que su teoría es acertada(25). También observa que al reemplazar los alimentos con harina de trigo por otros que contienen harina o almidón de maíz, o harina de arroz, reaparece el apetito en los pacientes y mejora la absorción de grasa, llegando incluso a desaparecer la esteatorrea.
En 1956 se realizan las primeras biopsias intestinales(26), comprobándose posteriormente que el gluten altera la mucosa intestinal de los celíacos, algo que redunda y apoya las tesis de Dicke. Por tanto se puede considerar a Willem Karel Dicke el pionero en la “Dieta sin gluten” de los niños celíacos.
Mientras que Dicke demuestra que una dieta sin gluten es el tratamiento adecuado para la EC, en Norteamérica prefieren seguir las prácticas del doctor Sidney V. Hass y su dieta de las bananas. Esta dieta se basa en reducir el aporte de hidratos de carbono procedentes de alimentos convencionales de los que estarían excluidas las bananas(27). Su tesis se basa en un estudio que realiza en pacientes celíacos a los que somete a una estricta dieta a base de bananas y leche suplementada con gelatina de caldo y un poco de carne. De los diez pacientes tratados, ocho mejoran espectacularmente y Haas publica en 1924(18) los resultados atribuyendo todo el mérito a las bananas porque, según él, contienen una enzima especial capaz de hidrolizar el almidón. Si bien, creemos necesario señalar, que la no eliminación de las bananas en la dieta de Haas pudiera deberse también, entre otros aspectos, a la sustitución “económicamente obligada” de alimentos ricos en hidratos de carbono menos asequibles por su alto precio, tras la crisis económica americana, por otros muy habituales y mucho más baratos como las bananas(28). Tampoco puede descartarse, aunque no hay referencia de este hecho, que la inclusión de las bananas se debiera a la observación de una baja incidencia de EC en los consumidores de dichos alimentos.
Pero no solo Haas recomienda el consumo de bananas para combatir la EC. En España, el pediatra Ángel Ballabriga Aguado publica en un artículo que “es más importante la eliminación o restricción al máximo de los hidratos de carbono de la dieta que la eliminación o el dar un régimen pobre en grasa”, aunque la restricción “debe ser para determinados hidratos de carbono”, de hecho, establece que el consumo de hidratos de carbono ha de ser en forma de disacáridos. Propone retirar los cereales de la dieta “con objeto de evitar o reducir al mínimo la fermentación hidrocarbonada, que es causa de distensión abdominal y diarrea” y pondera las bondades de una dieta a base de bananas, algarrobas y babeurre(29).
Por otra parte, en la primera mitad del siglo XX el interés sobre la EC se centra en los niños. Esto se debe a que los niños celíacos, respecto a los adultos, responden más rápidamente, y de forma mucho más espectacular, a los tratamientos dietéticos. Así, los pediatras consiguen mayores logros en el tratamiento de la enfermedad, mientras que los médicos de los adultos conquistan los principales avances en el diagnóstico de la EC. La primera profesora de pediatría en el Reino Unido y pionera en el campo de la gastroenterología pediátrica, fue la australiana Charlotte Anderson(18,20). El equipo de esta pediatra extrae el almidón y otros componentes de la harina de trigo en 1949 y averigua que el contenido de ese extracto es el causante del daño en los enfermos celíacos(12). Con este descubrimiento se refuerza la teoría de Dicke y en 1950 el tratamiento de los pacientes con EC se basa en la “Dieta sin gluten”.
En una publicación de Lancet en 1952, Anderson demuestra que el gluten del trigo y del centeno es la sustancia responsable de los daños en la EC(30). Esta teoría se confirma en 1953 por los holandeses Weijers y Van de Kamer(20).
Así mismo y conjuntamente con el descubrimiento de Dicke, el médico inglés J.W. Paulley de Ipswich comunica a la Sociedad Británica de Gastroenterología en Birmingham la causa del síndrome celíaco. Paulley encuentra una anormalidad de la mucosa del intestino delgado en una intervención quirúrgica a un paciente celíaco; dicha anormalidad consiste en la inflamación del intestino con pérdida de vellosidades(31). Este proceso inflamatorio, de naturaleza desconocida, se observa en varios pacientes más del doctor inglés y de otros médicos de otros países como Estados Unidos. Con este nuevo dato se obtiene información muy importante para diagnosticar y tratar la EC. Dicha inflamación radica en la pérdida de proyecciones microscópicas o vellosidades. Al ser estas vellosidades las responsables de la absorción de los nutrientes de los alimentos en el intestino para ser trasladados a la corriente sanguínea, su disminución conlleva alteraciones en la digestión en la publicación “Todo sobre la enfermedad celíaca”(32).
En 1962, se descubre que el linfoma de intestino delgado es una consecuencia de la EC. Al día de hoy, se sabe que la EC está detrás de muchos de estos linfomas y otros tipos de cáncer (adenocarcinoma de intestino delgado, linfomas de esófago o de faringe) relacionados directamente con las ulceraciones que se producen en el intestino delgado debidas a la destrucción de las vellosidades intestinales(33).
En la década de los años 60 del siglo pasado se observa `por primera vez que existe una tendencia a padecer la enfermedad dentro de una misma familia y se inician estudios de marcadores genéticos. Esta ‘tendencia familiar’ se muestra con especial claridad en gemelos monocigóticos, donde se da una concurrencia del 75%(34). Los primeros estudios en antígenos de leucocitos (antígenos de histocompatibilidad o HLA) sugirieron una relación con HLA B8 y más tarde mostraron una mayor prevalencia de A1 y B8 en celiacos que en controles, lo que evidenció que existe una minoría de celiacos que también tiene dichos HLA(35-37). Los avances en el conocimiento de la genética señalan claramente que existe una asociación primaria entre la celiaquía y algunos haplotipos -conjunto de alelos de riesgos que se heredan juntos y permiten la más fácil identificación de la relación entre mutación y enfermedad-. Así hay una relación primaria entre EC y el heterodímero HLA-DQ a/b codificado por los alelos HLA-DQ2 (DQA1*0501 y DQB1*0201). En España y países colindantes el 90% de los pacientes con enfermedad celíaca y el 20% de los individuos sanos presentan dicho haplotipo. Además, la mayoría de los pacientes DQ2 negativos presentan el haplotipo HLA-DQ8 (DQA1*0301 y DQB1*0302)(9).
Aunque en 1958 se relaciona por primera vez la EC con una reacción inmunológica al detectar anticuerpos circulantes(38), la relación entre EC y antígenos circulantes específicos no tiene lugar hasta 1983(39). Este hallazgo es crucial para utilizar técnicas de detección no invasivas y menos agresivas que la empleadas hasta entonces. De hecho las pruebas serológicas son de gran utilidad para la identificación de enfermos celiacos, teniendo especial interés la identificación y cuantificación de IgA antiendomisio por ser notablemente sensible (más del 90%) y específica (sobre el 90%) para CD. En 1997 se identifica a la transglutaminasa tisular como el antígeno en el endomisio que actúa como autoantígeno responsable de la CD (40), sin embargo quedan pendiente comprobar la posibilidad de la presencia de falsos positivos en otras lesiones intestinales(20).
En 1992, el profesor Michael N. Marsh de Oxford y sus colaboradores investigan las lesiones duodenales desde un punto de vista histológico (Figura 8). Así establecen cuatro estadios (I a IV o 1 a 4) según la intensidad de la lesión y los daños en el tejido van desde unos cambios mínimos en las vellosidades hasta lesiones que afectan intraepitelialmente(41).
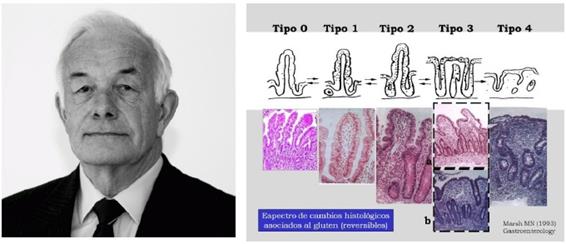
Figura 8. Profesor Michael Newton Marsh y la enfermedad celiaca. a) Michael
Newton Marsh. Foto de libre acceso; B) Estadios de Marsh dependiendo del
grado de lesión de la mucosa intestinal asociados a la ingesta de gluten. 0: Mucosa preinfiltrativa;
I: Aumento de Linfocitos intraepiteliales; II: Hiperplasia de las criptas; III a:
Atrofia vellositaria parcial; III b: Atrofia vellositaria total; IV: Atrofia vellositaria e
hipoplasia críptica.
htpps://www.bing.com/images/search?q=Estadios+de+Marsh+fotos&go=Buscar&qs=d
s&form=QBIDMH
Paralelamente surge el concepto de ‘iceberg de la enfermedad celíaca’ (Figura 9). Esta expresión se utiliza para describir, muy gráficamente, la incidencia de la EC, donde la parte visible de ese alegórico iceberg serían los casos de EC diagnosticados donde los síntomas son prueba evidente de que se padece la enfermedad, mientras que la parte no visible del iceberg (y mucho más grande que la visible) serían los casos no diagnosticados donde la enfermedad se muestra silente o simplemente en un estado potencial de desarrollarse. Aunque en el esquema presentamos un iceberg con dos sesiones, se han propuesto diferentes tipos como el de Logan, Catassi, Mäki, Feighery con tres o más sesiones donde se detallan tipos de EC (clásica, silente, etc.,) diagnóstico, síntomas y tratamientos(20).
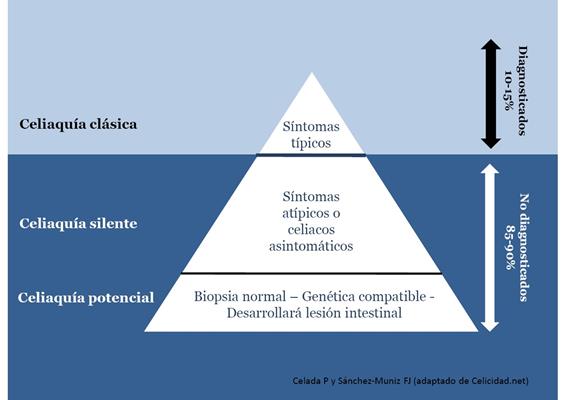 Figura 9. Representación
simplista del “Iceberg de la enfermedad celiaca” Modificado
Figura 9. Representación
simplista del “Iceberg de la enfermedad celiaca” Modificado
de www. celicidad.net Celicidad APP.
Una muestra evidente de la importancia y de la incidencia de la EC es el interés que están mostrando las autoridades sanitarias en la detección precoz de esta enfermedad, pues un diagnóstico temprano de la celiaquía puede evitar que se desarrollen los aspectos más negativos de esta dolencia.
A este respecto tenemos la obligación de citar que en 1968 se funda la Sociedad Celiaca del Reino Unido (originalmente Sociedad Celiaca) por Elizabeth Segall madre de un niño celíaco y Pedro Benenson, celíaco y uno de los fundadores de la organización de derechos humanos Amnistía Internacional, además el profesor Christopher C. Booth proporciona asesoramiento y asistencia médica inicial a dicha sociedad. En 1969 diversas organizaciones celíacas se establecen en California, Estados Unidos, y poco después en Canadá. Algunos años después se funda la Asociación de Sociedades Celíacas Europeas (AOECS).
El 25 de junio de 1994 se constituye la Federación de Asociaciones de Celiacos de España (FACE). FACE está constituida por 17 asociaciones de celiacos distribuidas por toda la geografía nacional. El objetivo fundamental de la FACE es coordinar el esfuerzo y la labor realizada por los miembros para defender sus derechos, con vistas a la unidad de acción y para un mejor logro de los fines comunes. Esta federación trabaja para mejorar la calidad de vida de las personas celiacas y conseguir su integración social. Esto lo realiza a través del apoyo directo a las personas celiacas y sus familiares, la realización de campañas de difusión y concienciación, la investigación, y la seguridad alimentaria.
En 2008 el Ministerio de Sanidad y Consumo a través de la Agencia Española de Seguridad Alimentaria y Nutrición (AESAN) presentan Nuevo Protocolo de Detección Precoz de la Celiaquía(42) donde se incluye una guía detallada sobre Diagnóstico Precoz de la Enfermedad Celíaca, editada por la Dra. Polanco(9). Con esta guía se pretende que los profesionales sanitarios estén al tanto de todos los posibles síntomas en que puede mostrarse la celiaquía y así poder detectar más tempranamente esta enfermedad. Un diagnóstico precoz conlleva no solo ventajas para el paciente, lo más importante, sino un ahorro en el gasto sanitario y laboral.
La detección de anticuerpos específicos en sangre en el año 2011 obliga a crear una nueva definición de intolerancia al gluten. En concreto, la presencia de anticuerpos anti-transglutaminasa en sangre es la consecuencia de su aparición previa en la mucosa del intestino, dando lugar a un nuevo método de detección de EC aunque la técnica para detectar este tipo de anticuerpos es sumamente compleja y aún no se la considera una práctica generalizada en clínica(12,43).
Como se comentó anteriormente, el tratamiento adecuado para la EC es una estricta dieta sin gluten, pero hasta la fecha evaluar el cumplimiento de dicha dieta es complicado pues no hay ningún método fiable que permita saber si la “Dieta sin gluten” se sigue de manera rigurosa. Además muchos clínicos no son partidarios de que se realicen nuevas biopsias para el seguimiento de la enfermedad. Debe recalcarse que tanto los cuestionarios rellenados por los propios pacientes, como las biopsias duodenales o la determinación de anticuerpos específicos no aportan una información detallada y por ello no son totalmente precisos para el dicho seguimiento de la “mejoría” de la enfermedad(43-46).
En palabras de Newnham(46) “Una debilidad significativa de todos los estudios clínicos sobre enfermedad celíaca hasta la fecha ha sido la ausencia de una medida objetiva del cumplimiento dietético. Los anticuerpos celíacos, la histología intestinal y los síntomas son todos herramientas imperfectas para la evaluación de la adherencia”.
Que no existan síntomas digestivos o que no se encuentren anticuerpos específicos no garantiza que la mucosa intestinal se esté recuperando. Además, la evaluación de esta mucosa mediante la técnica invasiva de la biopsia es muy complicada. Y es que la EC puede darse con cambios mínimos que no siempre van acompañados de degeneración de las vellosidades y por tanto son complicados de detectar(45). Sin embargo, y como no podía ser de otra manera, la experimentación continúa y se sigue investigando en nuevos métodos de detección. De hecho, desde el año pasado se dispone de un método de detección de gluten en orina y/o en heces para uso de profesionales y que en el año en curso ya puede adquirirse para uso doméstico(45).
En la Figura 10 hemos resumido el largo camino de la EC, señalando algunos de los personajes e hitos más relevantes. Queda ya muy lejos aquel siglo I d. C cuando Areteo de Capadocia diagnosticó muy básicamente la EC por primera vez, pero gracias a sus observaciones y al trabajo de quienes le sucedieron en el tiempo hoy se conoce mejor esta enfermedad pudiendo detectarla cada vez de manera más precoz, paliando en gran medida sus efectos deletéreos. La batalla contra la EC continúa, y si bien aún no se consigue derrotarla sí se la domina en la mayoría de los casos, consiguiendo una mejor calidad de vida para quienes la padecen.
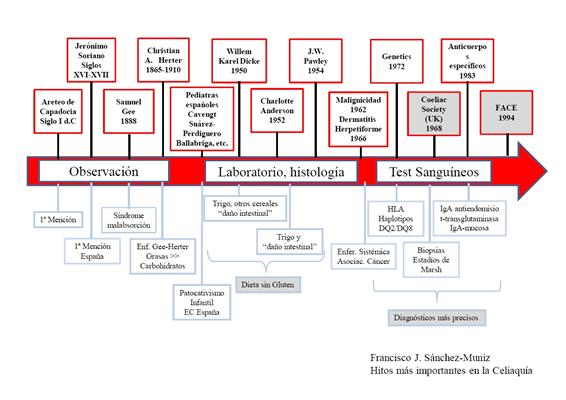
Figura 10. Esquema donde se incluyen los personajes e hitos más importantes
relacionados con la investigación de la enfermedad celiaca.
Agradecimientos
Este trabajo ha sido subvencionado gracias al proyecto del Ministerio de Economía y Competitividad en la convocatoria de Retos Investigación: Proyectos de I+D+i 2014 AGL 2014-53207-C2-2-R.
Referencias
1. Leffler DA, Green PH, Fasano A. Extraintestinal manifestations of coeliac disease. Nat Rev Gastroenterol Hepatol. 2015; 12(10): 561-567.
2. Lundin KE, Wijmenga C. Coeliac disease and autoimmune disease-genetic overlap and screening. Nat Rev Gastroenterol Hepatol. 2015; 12(9): 507-515.
3. Polanco, I; Larrauri, J. Does transient gluten intolerance exist? En: Kumar PJ, Walker-Simyh JA. (Eds). Coeliac disease: one hundred years. Middlesex. Leeds University Press. 1990; pp. 226-230.
4. Troncone, R; Auricchio,S. Coeliac disease. En: Wyllie R, Hyamans SS. (Eds.). Pediatric gastrointestinal disease. Filadelfia. Decker 1993; pp. 544-561.
5. Tovoli F, Masi C, Guidetti E, Negrini G, Paterini P, Bolondi L. Clinical and diagnostic aspects of gluten related disorders. World J Clin Cases. 2015; 3(3): 275-284.
6. Penagini F, Dilillo D, Meneghin F, Mameli C, Fabiano V, Zuccotti GV. Gluten-free diet in children: an approach to a nutritionally adequate and balanced diet. Nutrients 2013; 5(11): 4553-4565.
7. Kupper C. Dietary guidelines and implementation for celiac disease. Gastroenterol. 2005; 128(4 Suppl 1): S121-S127.
8. Rodrigo L, Garrote JA, Vivas S. Enfermedad Celíaca. Med Clin (Barc). 2008; 131(7): 264-270.
9. Polanco Allué I. (2008). Diagnóstico precoz de la enfermedad celíaca. Ministerio de Sanidad y Consumo (Ed.) Madrid, España.
10. Ciccocioppo R, Kruzliak P, Cangemi GC, Pohanka M, Betti E, Lauret E, Rodrigo L. The Spectrum of Differences between Childhood and Adulthood Celiac Disease. Nutrients 2015; 7(10): 8733-8751.
11. Molberg O, Mcadam SN, Körner R, Quarsten H, Kristiansen C, Madsen L, Fugger L, Scott H, Norén O, Roepstorff P, Lundin KE, Sjöström H, Sollid LM. Tissue transglutaminase selectively modifies gliadin peptides that are recognized by gut-derived T cells in celiac disease. Nat Med. 1998; 4(6):713-717.
12. Tommasini A, Not T, Ventura A. Ages of celiac disease: from changing environment to improved diagnostics. World J Gastroenterol. 2011; 17(32): 3665-3671
13. Nadhem ON, Azeez G, Smalligan RD, Urban S. Review and practice guidelines for celiac disease in 2014. Postgrad Med. 2015; 127(3): 259-265.
14. Woodward J. Improving outcomes of refractory celiac disease - current and emerging treatment strategies. Clin Experimen Gastroenterol. 2016; 9: 225-236.
15. Fasano A, Catáis C, Current approaches to diagnosis and treatment of celiac disease an evolving spectrum. Gastroenterology 2001; 120: 636-651.
16. Fasano A. Should we screen for coeliac disease? Yes. BMJ. 2009; 339: b3592.
17. García Almeida JM, García Alemán J, Martínez Alfaro B, Vilchez López FJ, Maraver Selfa S. Enfermedad celiaca, dieta controlada en gluten. En: de Luis Román D A, Bellido Guerrero D, García Luna PP. (Eds.). Dietoterapia, Nutrición Clínica y Metabolismo. Ed: Díaz de Santos. Madrid. 2012; pp. 247-249.
18. García Nieto VM. Historia de la enfermedad celíaca. En: Rodrigo L, Peña AS. (Eds.). Enfermedad celíaca y sensibilidad al gluten no celíaca. OmniaScience. Barcelona, España: 2013; pp. 45-59.
19. Vogten AJ, Peña AS. Coeliac disease: one century after Samuel Gee (1888). Neth J Med. 1987; 31(5-6): 253-255.
20. Losowsky MS. A history of coeliac disease. Dig Dis. 2008. 26(2); 112-120.
21. https://www.farodevigo.es/opinion/2013/11/24/enfermedad-celiaca-ayer/920266.html
22. Cavengt S. Infantilismo o patocativismo. En: Endocrinología infantil. Ruiz Hermanos eds. Madrid. 1922; pp. 131-170.
23. Cavengt S. Consideraciones clínicas sobre la celiaquia. Acta Ped Esp. 1950; 8: 199.
24. Suárez Perdiguero M. Enfermedad celíaca y síndrome celíaco. Concepto y patogénesis. Rev Esp Pediatr. 1945; 1: 683-695.
25. Dicke Wk, Weijers HA, Van De Kamer JH. Coeliac disease. II. The presence in wheat of a factor having a deleterious effect in cases of coeliac disease. Acta Paediatr. 1953; 42(1): 34-42.
26. Shiner M. Duodenal biopsy. Lancet 1956; 1: 17-19.
27. Abel EK. The rise and fall of celiac disease in the United States. J Hist Med Allied Sci. 2010; 65(1): 81-105.
28. 28 https://culturacientifica.com/2015/06/25/celiaquia-platanos-y-golpes-de-estado/
29. Ballabriga Aguado A. Tratamiento de la enfermedad celíaca con especial consideración a sus aspectos dietéticos. Acta Ped Esp. 1949; 7: 1519-1541.
30. Anderson CM, French JM, Sammons HG, Frazer AC, Gerrard JW, Smellie JM. Coeliac disease; gastrointestinal studies and the effect of dietary wheat flour. Lancet 1952; 1(17): 836-842.
31. Paulley JW Observation on the aetology of idiopathic steatorrhoea; jejunal and lymphnode biopsies. Br Med J. 1954; 2(4900): 1318-1321.
32. Márquez Infante M. Historia de la enfermedad celiaca. En: Asociación de Celíacos de Madrid. Consejería de Sanidad y Consumo. Todo sobre la enfermedad celiaca. 2008 www.celiacosmadrid.org
33. Catassi C, Bearzi I, Holmes GK. Association of celiac disease and intestinal lymphomas and other cancers. Gastroenterology 2005; 128(4 Suppl 1): S79-S86.
34. Ellis J: Coeliac disease and other gluten-sensitive disorders. En: Buttriss J (ed): Adverse Reactions to Food. Blackwell Science, London. 2002; pp 112-130.
35. Falchuk ZM, Rogentine GN, Strober W: Predominance of histocompatibility antigen HL-A8 in patients with gluten-sensitive enteropathy. J Clin Invest. 1972; 51: 1602-1605.
36. Stokes PL, Asquith P, Holmes GK, Mackintosh P, Cooke WT. Histocompatibility antigens associated with adult coeliac disease. Lancet 1972; 2: 162-164.
37. Granditsch G, Ludwig H, Polymenidis Z, Wick G. Letter: Coeliac disease and HL-A8. Lancet 1973; 2(7834): 908-909.
38. Berger E: Allergic pathogenesis of celiac disease with studies of the splitting up of pathogenic antigens by enzymes. Bibl Paediatr. 1958; 67: 1-55.
39. Chorzelski TP, Sulej J, Tchorzewska H, Jablonska S, Beutner EH, Kumar V. IgA class endomysium antibodies in dermatitis herpetiformis and celiac disease. Ann NY Acad Sci. 1983; 420: 325-334.
40. Dieterich W, Ehnis T, Bauer M, Donner P, Volta U, Riecken EO, Schuppan D. Identification of tissue transglutaminase as the autoantigen of celiac disease. Nat Med. 1997; 3: 797-801.
41. March MN. Gluten sensitivity and latency: can patterns of intestinal antibody secretion define the great 'silent majority?'. Gastroenterology. 1993; 104(5):1550-
42. Ministerio de Sanidad y Política Social. Nuevo protocolo de detección precoz de la celiaquía. Boletín impacto. DG Agencia de Calidad del SNS. Marzo 2018.
43. Molina-Infante J, Santolaria S, Sanders DS, Fernández-Bañares F. Systematic review: noncoeliac gluten sensitivity. Aliment Pharmacol Ther. 2015; 41(9): 807-820.
44. Moreno ML, Rodríguez-Herrera A, Sousa C, Comino I. Biomarkers to monitor gluten-free diet compliance in celiac patients. Nutrients 2017; 6(9): 1.
45. Syage JA, Kelly CP, Dickason MA, Ramirez AC, Leon F, Dominguez R, Sealey-Voyksner JA. Determination of gluten consumption in celiac disease patients on a gluten-free diet. Am J Clin Nutr. 2018; 107(2): 201-207.
46. Newnham ED. Coeliac disease in the 21st century: paradigm shifts in the modern age. J Gastroenterol Hepatol. 2017; 32(Suppl 1): 82-85.
